No es cierto que la vacuna de Pfizer produzca efectos secundarios graves o anómalos. Tampoco es cierto que las autoridades sanitarias de Reino Unido hayan aconsejado no vacunarse a todas las personas con algún tipo de alergia. Tampoco es cierto que la vacuna se haya empezado a administrar antes de saber todos los datos de seguridad.
La desinformación sobre la seguridad de la primera vacuna contra la COVID-19 ha calado muy bien y muy rápido. Uno de los motivos es que se parece lo suficiente a la verdad, es como información deforme.
Cuando se autoriza una vacuna significa que los beneficios superan a los riesgos. Hay que comunicar los riesgos con transparencia, pero sin dejar de lado la responsabilidad informativa. La realidad es que esta vacuna sí está contraindicada en personas que hayan padecido anafilaxia o episodios graves de alergia, y también produce algunos efectos secundarios, aunque estos son leves y parecidos a los que produce cualquier otra vacuna. Lo que de ninguna manera tiene un ápice de verdad, es que esta vacuna se haya autorizado a las carreras, o antes de tener todos los datos.
Cómo se ha evaluado la seguridad de la vacuna
La seguridad de una vacuna, tanto de la COVID-19 como de cualquier otra vacuna, se suele saber entre las seis y ocho primeras semanas de los ensayos clínicos. Es extremadamente raro que una vacuna produzca algún efecto secundario tiempo después, a medio o largo plazo, principalmente porque a nivel químico y biológico cumplen una única misión muy concreta y acotada en el tiempo.
Las agencias reguladoras, que son las encargadas de autorizar las vacunas y revisar que estas cumplen con los criterios exigidos de seguridad y eficacia, en lugar de esperar a que los ensayos clínicos terminasen, han ido haciendo una revisión continua. Esto ha permitido agilizar la autorización de las vacunas sin saltarse ninguna de las etapas del protocolo normal.
Los ensayos clínicos de las vacunas para la COVID-19 se someten a lo que se conoce como ‘revisión continua’ o rolling view. La rolling view es una de las herramientas regulatorias que utiliza la Agencia Europea del Medicamento (EMA) para acelerar la evaluación de un medicamento o vacuna prometedora durante una emergencia de salud pública.
En lugar de esperar a que se terminen los ensayos clínicos para revisar todos los resultados, en una rolling view hay un comité independiente de expertos en medicamentos de la EMA que va revisando los datos de eficacia, seguridad y calidad de la vacuna a medida que se producen. Una vez que el comité decide que hay suficientes datos disponibles como para formarse una opinión acerca de la idoneidad de la vacuna, la empresa puede presentar la solicitud formal de autorización. La EMA concluirá su evaluación durante una reunión extraordinaria programada para el 29 de diciembre a más tardar. Esta herramienta de revisión permite agilizar los trámites, por lo que es especialmente útil en momentos de emergencia sanitaria como el actual.
Las agencias reguladoras de otros territorios que ya han autorizado la vacuna lo han hecho a través de herramientas de la misma naturaleza. Esa es la razón por la que la primera campaña de vacunación para la COVID-19 de Reino Unido comenzó el 8 de diciembre con la vacuna de Pfizer, dos días antes de que el estudio científico completo se publicase en una revista científica, que es el cauce convencional por el que los datos se ponen al alcance de toda la comunidad científica.
El 10 de diciembre se publicaron los resultados de los ensayos clínicos de la vacuna de Pfizer y BioNTech en la revista científica The New England of Medicine. Esto significa que todos los datos han sido revisados por la comunidad científica, lo que se conoce como ‘revisión por pares’ o peer review.
Para evaluar la seguridad de la vacuna, los participantes del ensayo clínico llevaron un diario electrónico a través del cual informaban de todos los efectos desde la administración de la primera dosis (de la vacuna o del placebo) hasta 14 semanas después de la segunda dosis. Así se registra el tipo y la gravedad de los eventos secundarios, así como del uso de analgésicos (medicamentos para el dolor) o antipiréticos (medicamentos para la fiebre) que hayan tomado para tratar esos efectos.
Diferencia entre reacción alérgica leve y anafilaxia
En Reino Unido se han registrado tres casos de reacción alérgica tras la administración de la vacuna de Pfizer, según la agencia reguladora de medicamentos de Reino Unido Medicines and Healthcare products Regulatory Agency (MHRA). Dos fueron casos de anafilaxis, esto son reacciones alérgicas graves inmediatas, y otro fue una reacción alérgica leve. Por este motivo la MHRA ha aconsejado no vacunarse a personas con antecedentes de anafilaxia. Estas personas suelen tener que llevar encima autoinyectores de adrenalina. También ha aconsejado no administrar la segunda dosis de la vacuna a aquellas personas que hayan sufrido anafilaxia tras la primera dosis.
Si la anafilaxia pone en riesgo inmediato y repentino la vida del paciente se utiliza el término 'choque anafiláctico'. Para hacernos una idea, estas son las peligrosas reacciones repentinas que se producen en personas alérgicas a los frutos secos, al veneno de avispa, a algunos antiinflamatorios o antibióticos, o al látex.
El suceso ha tenido tal repercusión mediática, que da la impresión de que las reacciones alérgicas son un efecto secundario común de la vacuna de Pfizer. No es así. Según el informe de la FDA, solo el 0,6% de los vacunados en la fase 3 del ensayo clínico padecieron alguna reacción alérgica.
Según el prospecto de la vacuna facilitado por la MHRA "no se debe administrar la vacuna si es alérgico al principio activo o a cualquiera de los demás componentes de este medicamento". El principal componente de la vacuna es el ARN mensajero, mientras que el resto son excipientes de uso común, lo que explicaría la baja incidencia de las reacciones alérgicas.
En conclusión, las personas que no padecen ninguna alergia grave conocida, sin antecedentes de anafilaxia, sí podrán vacunarse.
Reacciones locales de la vacuna
Las reacciones locales son los efectos derivados de la inyección, como dolor, hinchazón, enrojecimiento o picor en el lugar de la inyección.
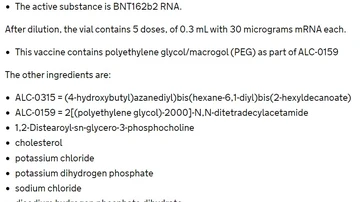
En general, los receptores de la vacuna informaron de más reacciones locales que los receptores de placebo, según el estudio publicado en NEJM. Entre los vacunados, el dolor leve a moderado en el lugar de la inyección dentro de los 7 días posteriores a la inyección fue la reacción local informada con mayor frecuencia. Menos del 1% de los participantes informaron de dolor severo.
El dolor se informó con menos frecuencia entre los participantes mayores de 55 años (71% tras la primera dosis; 66% tras la segunda dosis) que entre los participantes más jóvenes (83% tras la primera dosis; 78% tras de la segunda dosis).
Un porcentaje notablemente menor de participantes informó de enrojecimiento o hinchazón en el lugar de la inyección. La proporción de participantes que informaron reacciones locales no aumentó después de la segunda dosis, y ningún participante informó de una reacción local de grado 4, que sería la de mayor gravedad.
En general, las reacciones locales fueron en su mayoría de intensidad leve a moderada y desaparecieron en menos de 2 días.
Reacciones sistémicas de la vacuna
Las reacciones sistémicas notificadas con más frecuencia fueron fatiga y dolor de cabeza (59% y 52%, respectivamente a cada dosis, entre los receptores de la vacuna más jóvenes; 51% y 39% entre los receptores de mayor edad). Aunque muchos receptores de placebo también informaron de fatiga y dolor de cabeza (23% y 24% entre los más jóvenes; 17% y 14% entre los de mayor edad).
Los eventos sistémicos fueron informados con más frecuencia por los receptores de la vacuna más jóvenes (de 16 a 55 años) que por los receptores de la vacuna de mayor edad (más de 55 años) y con más frecuencia después de la segunda dosis 2 que de la primera.
Las reacciones de fatiga y dolor de cabeza consideradas graves afectaron respectivamente al 3,8% y 2% de pacientes tras recibir la segunda dosis. El malestar pudo subsanarse con analgésicos.
Se informó de fiebre por encima de 38 °C después de la segunda dosis en el 16% de los receptores de la vacuna más jóvenes y en el 11% de los mayores. Dos participantes en los grupos de vacuna y otros dos del grupo placebo tuvieron fiebre por encima de los 40 °C.
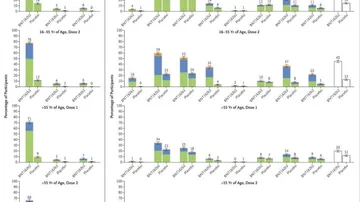
Los receptores de la vacuna más jóvenes utilizaron más analgésicos y antipiréticos para tratar estos efectos (28% y 45% después de cada dosis) que los receptores de la vacuna de mayor edad (20% y 38%). Los receptores de placebo utilizaron menos medicamentos (10% y 14%) que los receptores de la vacuna, independientemente de la edad o la dosis.
Estas reacciones sistémicas aparecieron durante los dos primeros días tras la administración de la vacuna, y desaparecieron a los pocos días.
Efectos adversos de la vacuna
Los efectos adversos son los problemas médicos inesperados. Todos los participantes del ensayo clínico (para la vacuna de Pfizer fueron 43.252 personas) deben informar de cualquier cambio en su estado de salud, a fin de confirmar si la vacuna está relacionada. Solo cuatro de los 43.252 participantes del ensayo clínico sufrieron efectos considerados graves, ninguno de ellos resultó mortal. Es un buen dato de seguridad.
Más receptores de la vacuna que los que recibieron placebo informaron de algún evento adverso (27% y 12%, respectivamente), según el artículo publicado en NEJM. 64 receptores de la vacuna (0,3%) y 6 receptores de placebo (<0,1%) informaron de adenopatía (inflamación de los ganglios linfáticos). Cuatro receptores de la vacuna (<0,1%) sufrieron efectos considerados graves: lesión en el hombro relacionada con la administración de la vacuna, linfadenopatía axilar derecha, arritmia ventricular paroxística y parestesia de la pierna derecha.
Durante el ensayo clínico fallecieron dos receptores de vacuna, uno por arteriosclerosis y otro por paro cardíaco; y cuatro receptores de placebo, dos por causas desconocidas, uno por accidente cerebrovascular hemorrágico y uno por infarto de miocardio. Los investigadores consideraron que ninguna muerte estaba relacionada con la vacuna o el placebo. Tampoco se observaron muertes asociadas a COVID-19.
El control de seguridad continuará durante 2 años después de la administración de la segunda dosis de vacuna.
Embarazo, lactancia, menores y personas inmunodeprimidas
Los datos de seguridad sobre estos grupos son muy limitados o inexistentes. Esto es así fundamentalmente por razones biotéticas: en los ensayos clínicos participan personas sanas o cuyas características particulares previsiblemente no les pongan en riesgo. Por eso, por principio de precaución, no se está recomendando la vacunación en estos casos.
Según la MHRA, si estás embarazada o en periodo de lactancia, crees que podrías estar embarazada o tienes intención de quedarte embarazada, consulta a tu médico o farmacéutico antes de recibir esta vacuna. Como precaución, debes evitar quedarte embarazada hasta al menos 2 meses después de la vacuna.
Las personas con un sistema inmunológico debilitado, como debido a una infección por VIH, o que estén tomando un tratamiento crónico que suprima o prevenga las respuestas inmunitarias, también deben consultar antes con su médico. Es posible que la vacuna no sea efectiva en personas inmunodeprimidas.
No se recomienda para niños menores de 16 años. Esto es así porque no hay datos sobre ellos, en los ensayos clínicos no han participado menores.
Conclusiones
A la hora de autorizar cualquier medicamento se hace un balance de riesgos y beneficios y con ello las agencias reguladoras toman la decisión. Igual que cualquier medicamento, las vacunas producen efectos secundarios. Esta también. Todos ellos entran dentro de los efectos esperables en cualquier vacuna. Y como la incidencia es baja y la gravedad también es baja, los beneficios de autorizar la vacuna sobrepasan con creces a los riesgos. Esa al menos ha sido la decisión que han tomado las autoridades sanitarias de Estados Unidos y de Reino Unido, donde ya ha empezado la campaña de vacunación.
Según el informe de la vacuna de Pfizer de la FDA, los efectos secundarios fueron los habituales en casi cualquier vacuna. Los más comunes fueron reacciones en el lugar del pinchazo (84,1%), cansancio (62,9%), dolor de cabeza (55,1%), dolor muscular (38,3%), escalofríos (31,9%), dolor de articulaciones (23,6%) y fiebre (14,2%). En general, estas reacciones fueron entre leves y moderadas. Fueron más frecuentes tras la segunda dosis que tras la primera, y menos frecuentes en mayores de 55 años.
La vacuna es segura. Se puede afirmar con contundencia, pero ojo, también hay que ser transparentes con lo que significa esto. Que una vacuna sea segura significa que conocemos los efectos secundarios que causa pero hemos determinado que son asumibles, no significa que no los tenga.
Esto es muy importante porque la campaña de vacunación ya ha arrancado en algunos países y estas semanas se publicarán noticias sobre los efectos secundarios y entrevistas a gente vacunada que los haya padecido. La vorágine informativa puede inducir recelos hacia la vacuna. Pienso en los países en los que se está vacunando primero a la gente mayor, con más de 90 años. ¿Qué pasará cuando una de estas personas fallezca? ¿Cómo afectará todo esto a la disposición de la gente a vacunarse? En España hay muchas personas que desconfían de la seguridad de esta vacuna, que la rechazan o que no saben si se la pondrían.
Si la vacuna finalmente se autoriza en Europa, y en consecuencia se autoriza en España, hay que estar preparados para lidiar con el exceso de información y con la facilidad con la que esta se deforma. Por eso la transparencia es tan importante como la responsabilidad informativa.
