Desvelan los mecanismos que originan la leucemia pediátrica más común
Desvelan los mecanismos que originan la leucemia pediátrica más común
Científicos del Instituto de Investigación contra la Leucemia Josep Carreras revelan los mecanismos que provocan la leucemia linfoblástica aguda hiperdiploide, la leucemia de células B pediátrica más frecuente. Hasta la fecha se sabía muy poco sobre cómo se produce la hiperdiploidía en este tipo de cáncer infantil.

Publicidad
La leucemia linfoblástica aguda de células B (LLA-B) se caracteriza por la acumulación de precursores inmaduros anormales de células B en la médula ósea, y es el cáncer pediátrico más común.
Entre los diferentes subtipos, el más frecuente se caracteriza por la presencia de un número mayor de cromosomas que en las células sanas y se denomina LLA-B con hiperdiploidía alta –una anormalidad genética–. El 30 % de las LLA-B pediátricas son hiperdiploides. Suelen tener un pronóstico favorable, con una supervivencia del 90 %.
El 30 % de las leucemias linfoblásticas agudas de células B son hiperdiploides. Suelen tener un pronóstico favorable, con una supervivencia del 90 %
Hasta la fecha se sabía muy poco sobre cómo se produce la hiperdiploidía en este tipo de cáncer infantil, aunque sí se conocía su efecto iniciador tumoral como alteración secundaria necesaria para la acumulación de células B leucémicas en la médula ósea.
El equipo liderado por Óscar Molina, investigador del grupo de Células Madre, Biología del Desarrollo e Inmunoterapia del Instituto de Investigación contra la Leucemia Josep Carreras, ha descubierto los mecanismos fisiopatológicos relacionados con la hiperdiploidía de LLA-B pediátrica. Los resultados se publican en la revista Blood.
Los autores del estudio plantearon la hipótesis de que el origen de dichos mecanismos podía suceder en el momento en que la célula se divide: la mitosis, un proceso celular que controla la distribución equitativa del material genético, ya duplicado y compactado previamente en los cromosomas, y los reparte en dos células ‘recién nacidas’.
“Ya sabíamos que hiperdiploidía de este tipo de leucemia surge en un progenitor de células B en el útero. Sin embargo, los mecanismos moleculares seguían siendo un enigma. Observamos lo que sucedía justo en el momento de la segregación cromosómica en LLA-B hiperdiploide para encontrar una explicación a este proceso oncogénico”, explica Molina.
Desarrollo de terapias más específicas y menos tóxicas
Los investigadores usaron una gran cohorte de muestras pediátricas primarias de LLA-B de 54 pacientes. Descubrieron que tres procesos y factores clave para una correcta segregación cromosómica durante la división celular estaban dañados o inhibidos en las células hiperdiploides.
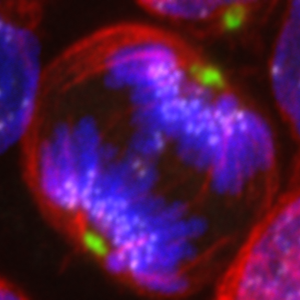
Célula leucémica B hiperdiploide dividiéndose con cromosomas repartiéndose. Imagen de microscopía confocal de una muestra de LLA-B teñida, con tubulina (rojo), pericentrina (verde), centrómeros (lila) y ADN (azul) . / Fcarreras
Además, comprobaron que la interrupción artificial de estos procesos en las células sanguíneas con números cromosómicos normales generaba células hiperdiploides parecidas a las de las muestras LLA-B.
Estos actores son el complejo de proteínas de la condensina, responsable de ayudar a condensar correctamente el material genético en los cromosomas; la proteína aurora B quinasa, responsable de que los cromosomas se unan correctamente para que acaben dirigiéndose a los polos opuestos de la célula que se divide en dos.
Es más, en el punto de control celular de este último proceso (conocido como SAC) también se han visto disfunciones. Con estos hallazgos, el equipo ha revelado los mecanismos moleculares que se alteran en este tipo frecuente de cáncer de sangre pediátrico.
“Los siguientes pasos serían estudiar si otros subtipos de LLA-B con números anormales de cromosomas, como el LLA-B hipodiploide, que es un subtipo muy agresivo de cáncer de sangre pediátrico, comparten un mecanismo molecular común”, apunta Molina.
“Estos estudios permitirán generar los primeros modelos preclínicos in vivo de leucemias con números anormales de cromosomas, cruciales para entender su origen y crecimiento. Esto facilitará el desarrollo y la prueba de terapias más específicas y menos tóxicas para estos cánceres sanguíneos pediátricos”, concluye.
Referencia:
Molina O, Vinyoles M, Granada I, Roca-Ho H, Gutierrez-Agüera F, Valledor L, Menéndez ST, Pal D, Paola Ballerini8, Monique den Boer9, Plensa, M, Perez-Iribarne M, Rodríguez-Perales S, Calasanz MJ, Ramírez-Orellana M, Rodríguez R, Camós M, Calvo M, Bueno C, Menéndez P. Impaired Condensin Complex and Aurora B kinase underlie mitotic and chromosomal defects in hyperdiploid B-cell ALL. Blood 2020. Doi: 10.1182/blood.2019002538
Esta investigación ha sido financiada principalmente por el Consejo Europeo de Investigación (CoG-2014-646903), el Ministerio de Economía y Competitividad (SAF-2016-80481-R), la Asociación Española Contra el Cáncer (AECC-CI-2015), y el ISCIII (PI17/01028). Óscar Molina ha recibido el apoyo del Lady Tata Memorial Trust (2017) y una beca postdoctoral "Beatriu de Pinós" (2018-2019) de la Generalitat de Catalunya (2016-BP00048).
Publicidad